Алкены общая формула и химическое строение. Основные реакции алкенов
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены). Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения , прежде всего водорода, с образованием предельных, или насыщенных, углеводородов - алканов.
Строение алкенов
Ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле С n Н 2n .
Свое второе название - олефины - алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров - масел (от англ. oil - масло).
Атомы углерода, между которыми есть двойная связь, находятся в состоянии sр 2 -гибридизации . Это означает, что в гибридизации участвуют одна s- и две р-орбитали, а одна р-орбиталь остается негибридизованной.

Перекрывание гибридных орбиталей приводит к образованию σ-связи, а за счет негибридизованных р-орбиталей соседних атомов углерода образуется вторая, π-связь. Таким образом, двойная связь состоит из одной σ- и одной π-связи .
Гибридные орбитали атомов, образующих двойную связь, находятся в одной плоскости, а орбитали, образующие π-связь, располагаются перпендикулярно плоскости молекулы.
Двойная связь (0,132 нм) короче одинарной, а ее энергия больше, т. к. она является более прочной. Тем не менее, наличие подвижной, легко поляризуемой π-связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.

Гомологический ряд алкенов
Первые три члена гомологического ряда алкенов газы, с C 5 H 10 до C 17 H 34 – жидкости, с C 18 H 36 – твердые вещества. Жидкие и твердые алкены практически нерастворимы в воде, но хорошо растворимы в органических растворителях.
В соответствии с правилами ИЮПАК, в названии гомологов ряда алкенов используется суффикс -ен. Положение двойной связи указывается с помощью цифры, обозначающей месторасположение связи. Цифра проставляется после названия основной цепи через дефис. Нумерация атомов в молекуле алкена начинается с того конца, к которому ближе связь, например, алкен, отвечающий формуле CH 3 −CH 2 −CH=CH−CH 3 следует называть пентен-2, поскольку связь начинается у второго атома углерода, начиная с конца цепи.
Неразветвленные алкены составляют гомологический ряд этена (этилена): С 2 Н 4 - этен, С 3 Н 6 - пропен, C 4 H 8 - бутен, С 5 Н 10 - пентен, С 6 Н 12 - гексен и т. д.
Изомерия и номенклатура алкенов
Для алкенов, так же как и для алканов, характерна структурная изомерия . Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, - это бутен.

Особым видом структурной изомерии является изомерия положения двойной связи:
Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение атомов углерода, поэтому молекулы алканов могут приобретать самую разнообразную форму. Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов еще одного вида изомерии - геометрической , или цис- транс-изомерии .

Цис-изомеры отличаются от транс-изомеров пространственным расположением фрагментов молекулы (в данном случае метильных групп) относительно плоскости π-связи, а следовательно, и свойствами.
Алкены изомерны циклоалканам (межклассовая изомерия), например:

Номенклатура алкенов, разработанная ИЮПАК, схожа с номенклатурой алканов.
1. Выбор главной цепи . Образование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи . Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь. Например, правильное название соединения:

5-метилгексен-2, а не 2-метилгексен-4, как можно было бы предположить.
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.

3. Формирование названия . Названия алкенов формируются так же, как и названия алканов. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс -ен, обозначающий принадлежность соединения к классу алкенов. Например:

Физические свойства алкенов
Первые три представителя гомологического ряда алкенов - газы; вещества состава С 5 Н 10 — С 16 Н 32 - жидкости; высшие алкены - твердые вещества.
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства алкенов
Реакции присоединения. Напомним, что отличительной чертой представителей непредельных углеводородов - алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения .
1. Гидрирование алкенов . Алкены способны присоединять водород в присутствии катализаторов гидрирования, металлов - платины, палладия, никеля:
Эта реакция протекает при атмосферном и повышенном давлении и не требует высокой температуры, т. к. является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция - дегидрирование.
2. Галогенирование (присоединение галогенов). Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (CCl 4) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов:
3. Гидрогалогенирование (присоединение галогеноводорода).
Эта реакция подчиняется правилу Марковникова :
При присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген - к менее гидрированному.
4. Гидратация (присоединение воды). Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта:
Обратите внимание на то, что первичный спирт (с гидроксогруппой при первичном углероде) образуется только при гидратации этена. При гидратации пропена или других алкенов образуются вторичные спирты.

Эта реакция протекает также в соответствии с правилом Марковникова - катион водорода присоединяется к более гидрированному атому углерода, а гидроксогруппа - к менее гидрированному.
5. Полимеризация . Особым случаем присоединения является реакция полимеризации алкенов:
Эта реакция присоединения протекает по свободнорадикальному механизму.
Реакции окисления.
1. Горение . Как и любые органические соединения, алкены горят в кислороде с образованием СО 2 и Н 2 О:

2. Окисление в растворах . В отличие от алканов алкены легко окисляются под действием растворов перманганата калия. В нейтральных или щелочных растворах происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:

Для алкенов наиболее характерны реакции, протекающие за счет раскрытия менее прочной π-связи. При этом π-связь (в исходном алкене) преобразуется в σ-связь в продукте реакции. Исходное ненасыщенное соединение превращается в насыщенное без образования других продуктов, т.е. происходит реакция присоединения .
По какому механизму идут реакции присоединения к алкенам?
1. За счет электронов π-связи в молекулах алкенов имеется область повышенной электронной плотности (облако π-электронов над и под плоскостью молекулы):
Поэтому двойная связь склонна подвергаться атаке электрофильным (электронодефицитным) реагентом. В этом случае будет происходить гетеролический разрыв π-связи и реакция пойдет по ионному механизму как электрофильное присоединение.
Механизм электрофильного присоединения обозначается символом Аd Е
(по первым буквам английских терминов: Ad – addition [присоединение],
Е - electrophile [электрофил]).
2. С другой стороны, углерод-углеродная π-связь, являясь неполярной, может разрываться гомолитически, и тогда реакция будет идти по радикальному механизму.
Механизм радикального присоединения обозначается символом Аd R
(R – radical - радикал).
Механизм присоединения зависит от условий проведения реакции.
Кроме того, алкенам свойственны реакции изомеризации и окисления (в том числе реакция горения , характерная для всех углеводородов).
Реакции присоединения к алкенам
Алкены вступают в разнообразные реакции присоединения.
1. Гидрирование (присоединение водорода)
Алкены взаимодействуют с водородом при нагревании и повышенном давлении в присутствии катализаторов (Pt, Pd, Ni и др.) с образованием алканов:
Гидрирование алкенов – реакция, обратная дегидрированию алканов . Согласно принципу Ле Шателье , гидрированию благоприятствует повышенное давление, т.к. эта реакция сопровождается уменьшением объёма системы.
Присоединение водорода к атомам углерода в алкенах приводит к понижению степени их окисления:
Поэтому гидрирование алкенов относят к реакциям восстановления. Эта реакция используется в промышленности для получения высокооктанового топлива.
2. Галогенирование (присоединение галогенов)
Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной температуре, без катализатора). Например, быстрое обесцвечивание красно-бурой окраски раствора брома в воде (бромной воды) служит качественной реакцией на наличие двойной связи:
Так, в реакции HCl c пропиленом из двух возможных структурных изомеров 1-хлорпропана и 2-хлорпропана, образуется последний:
Эта закономерность была первоначально установлена эмпирически. В современной органической химии дано теоретическое обоснование правила Марковникова на основе положения о влиянии электронного строения молекул на их реакционную способность.
Следует отметить, что правило Марковникова в его классической формулировке соблюдается только для электрофильных реакций самих алкенов. В случае некоторых производных алкенов или при изменении механизма реакции идут против правила Марковникова.
4. Гидратация (присоединение воды)
Гидратация происходит в присутствии минеральных кислот по механизму электрофильного присоединения:
В реакциях несимметричных алкенов соблюдается правило Марковникова.
1. Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера) по схеме:
n M M n
Число n в формуле полимера (M n ) называется степенью полимеризации. Реакции полимеризации алкенов идут за счёт присоединения по кратным связям:
2. Димеризация алкенов – образование димера (удвоенной молекулы) в результате реакции присоединения. В присутствии минеральной кислоты (донора протона Н + ) происходит присоединение протона по двойной связи молекулы алкена. При этом образуется карбокатион:
"Димерный карбокатион" стабилизируется путем выброса протона, что приводит к продуктам димеризации алкена – смеси изомерных диизобутиленов (2,4,4-триметипентена-2 и 2,4,4-триметилпентена-1):
Этот процесс протекает при обработке изобутилена (2-метипропена) 60% серной кислотой при температуре 70°С. Образовавшаяся в результате смесь диизобутиленов подвергается гидрированию с целью получения "изооктана" (2,2,4-триметилпентана), который применяется для улучшения антидетонационной способности бензина ("изооктан" – стандарт моторного топлива с октановым числом 100).
Содержащие пи-связь - это непредельные углеводороды. Они являются производными алканов, в молекулах которых произошло отщепление двух атомов водорода. Образовавшиеся свободные валентности формируют новый тип связи, которая располагается перпендикулярно плоскости молекулы. Так возникает новая группа соединений - алкены. Физические свойства, получение и применение веществ этого класса в быту и промышленности мы рассмотрим в этой статье.
Гомологический ряд этилена
Общая формула всех соединений, называемых алкенами, отражающая их качественный и количественный состав, - это C n H 2 n . Названия углеводородов по систематической номенклатуре имеют следующий вид: в термине соответствующего алкана изменяется суффикс с -ан на -ен, например: этан - этен, пропан - пропен и т. д. В некоторых источниках можно встретить еще одно название соединений этого класса - олефины. Далее мы изучим процесс образования двойной связи и физические свойства алкенов, а также определим их зависимость от строения молекулы.
Как образуется двойная связь
Электронную природу пи-связи на примере этилена можно представить следующим образом: атомы карбона в его молекуле находятся в форме sp 2 -гибридизации. В этом случае формируется сигма-связь. Еще две гибридные орбитали - по одной от атомов углерода, формируют простые сигма-связи с водородными атомами. Два оставшихся свободных гибридных облака атомов карбона перекрываются над и под плоскостью молекулы - образуется пи-связь. Именно она определяет физические и химические свойства алкенов, речь о которых пойдет далее.

Пространственная изомерия
Соединения, имеющие один и тот же количественный и качественный состав молекул, но различное пространственное строение, называются изомерами. Изомерия встречается в группе веществ, называемых органическими. На характеристику олефинов большое влияние оказывает явление оптической изомерии. Она выражается в том, что гомологи этилена, содержащие у каждого из двух углеродных атомов при двойной связи различные радикалы или заместители, могут встречаться в форме двух оптических изомеров. Они отличаются друг от друга положением заместителей в пространстве относительно плоскости двойной связи. Физические свойства алкенов в этом случае также будут разными. Например, это касается температур кипения и плавления веществ. Так, олефины неразветвленного строения углеродного скелета имеют более высокие температуры кипения, чем соединения-изомеры. Также температуры кипения цис-изомеров алкенов выше, чем транс-изомеров. В отношении температур плавления картина противоположная.
Сравнительная характеристика физических свойств этилена и его гомологов
Первые три представителя олефинов являются газообразными соединениями, затем, начиная с пентена C 5 H 10 и до алкена с формулой C 17 H 34 , - жидкости, а далее идут твердые вещества. У гомологов этена прослеживается следующая тенденция: температуры кипения соединений снижаются. Например, у этилена этот показатель равен -169,1°C, а у пропилена -187,6°C. Зато температуры кипения с увеличением молекулярной массы повышаются. Так, у этилена она равна -103,7°C, а у пропена -47,7°C. Подводя итог сказанному, можно сделать вывод, звучащий кратко: физические свойства алкенов зависят от их молекулярной массы. С ее увеличением изменяется агрегатное состояние соединений в направлении: газ - жидкость - твердое вещество, а также снижается температура плавления, а температуры кипения возрастают.

Характеристика этена
Первый представитель гомологического ряда алкенов - это этилен. Он является газом, малорастворимым в воде, но хорошо растворяющимся в органических растворителях, не имеющим цвета. Молекулярная масса - 28, этен немного легче воздуха, имеет едва уловимый сладковатый запах. Он легко вступает в реакции с галогенами, водородом и галогеноводородами. Физические свойства алкенов и парафинов тем не менее достаточно близки. Например, агрегатное состояние, способность метана и этилена к жесткому окислению и т. д. Как же можно различить алкены? Как выявить непредельный характер олефина? Для этого существуют качественные реакции, на которых мы и остановимся подробнее. Напомним, какую особенность в строении молекулы имеют алкены. Физические и химические свойства этих веществ определяются наличием в их составе двойной связи. Чтобы доказать ее присутствие, пропускают газообразный углеводород через фиолетовый раствор перманганата калия или бромную воду. Если они обесцветились, значит, соединение содержит в составе молекул пи-связи. Этилен вступает в реакцию окисления и обесцвечивает растворы KMnO 4 и Br 2 .
Механизм реакций присоединения
Разрыв двойной связи заканчивается присоединением к свободным валентностям карбона атомов других химических элементов. Например, при взаимодействии этилена с водородом, называемом гидрогенизацией, получается этан. Необходим катализатор, например порошковидный никель, палладий или платина. Реакция с HCl заканчивается образованием хлорэтана. Алкены, содержащие более двух атомов углерода в составе своих молекул, проходят реакцию присоединения галогеноводородов с учетом правила В. Марковникова.

Как гомологи этена взаимодействуют с галогеноводородами
Если перед нами стоит задание "Охарактеризуйте физические свойства алкенов и их получение", нам нужно рассмотреть правило В. Марковникова более подробно. Практическим путем установлено, что гомологи этилена реагируют с хлороводородом и другими соединениями по месту разрыва двойной связи, подчиняясь некоторой закономерности. Она заключается в том, что атом водорода присоединяется к наиболее гидрогенизированному углеродному атому, а ион хлора, брома или йода - к карбоновому атому, содержащему наименьшее количество атомов водорода. Эта особенность протекания реакций присоединения получила название правила В. Марковникова.
Гидратация и полимеризация
Продолжим далее рассматривать физические свойства и применение алкенов на примере первого представителя гомологического ряда - этена. Его реакция взаимодействия с водой используется в промышленности органического синтеза и имеет важное практическое значение. Впервые процесс был проведен еще в XIX веке А.М. Бутлеровым. Реакция требует выполнения ряда условий. Это, прежде всего, использование концентрированной серной кислоты или олеума в качестве катализатора и растворителя этена, давление порядка 10 атм и температура в пределах 70°. Процесс гидратации происходит в две фазы. Вначале по месту разрыва пи-связи к этену присоединяются молекулы сульфатной кислоты, при этом образуется этилсерная кислота. Затем полученное вещество реагирует с водой, получается этиловый спирт. Этанол - важный продукт, применяемый в пищевой промышленности для получения пластмасс, синтетических каучуков, лаков и других продуктов органической химии.

Полимеры на основе олефинов
Продолжая изучать вопрос применения веществ, относящихся к классу алкенов, изучим процесс их полимеризации, в котором могут участвовать соединения, содержащие непредельные химические связи в составе своих молекул. Известно несколько типов реакции полимеризации, по которым происходит образование высокомолекулярных продуктов - полимеров, например таких как полиэтилен, полипропилен, полистирол и т. д. Свободнорадикальный механизм приводит к получению полиэтилена высокого давления. Это одно из наиболее широко применяемых соединений в промышленности. Катионно-ионный тип обеспечивает получение полимера стереорегулярного строения, например полистирола. Он считается одним из наиболее безопасных и удобных в использовании полимеров. Изделия из полистирола устойчивы к агрессивным веществам: кислотам и щелочам, негорючие, легко окрашиваются. Еще один вид механизма полимеризации - димеризация, он приводит к получению изобутена, применяемого в качестве антидетонационной добавки к бензину.
Способы получения
Алкены, физические свойства которых мы изучаем, получают в лабораторных условиях и промышленности различными методами. В опытах в школьном курсе органической химии используют процесс дегидратации этилового спирта с помощью водоотнимающих средств, например таких, как пятиокись фосфора или сульфатная кислота. Реакция проводится при нагревании и является обратной процессу получения этанола. Еще один распространенный способ получения алкенов нашел свое применение в промышленности, а именно: нагревание галогенопроизводных предельных углеводородов, например хлорпропана с концентрированными спиртовыми растворами щелочей - гидроксида натрия или калия. В реакции происходит отщепление молекулы хлороводорода, по месту появления свободных валентностей атомов карбона образуется двойная связь. Конечным продуктом химического процесса будет олефин - пропен. Продолжая рассматривать физические свойства алкенов, остановимся на главном процессе получения олефинов - пиролизе.

Промышленное производство непредельных углеводородов ряда этилена
Дешевое сырье - газы, образующиеся в процессе крекинга нефти, служат источником получения олефинов в химической промышленности. Для этого применяют технологическую схему пиролиза - расщепление газовой смеси, идущее с разрывом углеродных связей и образованием этилена, пропена и других алкенов. Пиролиз проводят в специальных печах, состоящих из отдельных пирозмеевиков. В них создается температура порядка 750-1150°C и присутствует водяной пар в качестве разбавителя. Реакции происходят по цепному механизму, идущему с образованием промежуточных радикалов. Конечный продукт - это этилен или пропен, их получают в больших объемах.

Мы подробно изучили физические свойства, а также применение и способы получения алкенов.
1. Окисление алкенов.
1.1 Горение.
В избытке воздуха или кислорода все алкены сгорают до углекислого газа и воды:
СН 3 – СН = СН 2 + 4,5 О 2 3 СО 2 + 3 Н 2 О
Горение алкенов не применяется в двигателях внутреннего сгорания, так как при хранении бензина они осмоляются и смолы забивают топливную аппаратуру (инжектор).
Возможность горения алкенов следует учитывать при транспортировке и хранении на химических предприятиях.
1.2 Окисление алкенов расчётным количеством кислорода воздуха в присутствии серебра.
Эпоксидные соединения применяются для создания клеев различного назначения.
1.3 Окисление алкенов однопроцентным раствором перманганата калия в воде – качественная реакция на алкены Е.Е Вагнера.
Реакция впервые описана Е.Е. Вагнером в «Журнале русского физико-химического общества» в 1886 году. Окисление алкенов или других непредельных соединений происходит при комнатной температуре и сопровождается исчезновением фиолетовой окраски перманганат-иона и выпадением бурого осадка диоксида марганца..Вне зависимости от строения алкена (но не алкадиена, например) коэффициенты в реакции Вагнера всегда одинаковые (324-322). Ниже приведены примеры окисления конкретных алкенов и показаны полуреакции и суммарная ОВР в ионном и молекулярном виде:

 :
:
Как видно в реакции Вагнера конечными органическими продуктами являются двухатомные спирты. Они называются так же гликолями. Например, 1,2-этандиол называется этиленгликолем.
1.4 Окисление алкенов сильными окислителями в жидкой фазе в кислой среде.
В зависимости от строения алкенов при окислении в этих условиях получаются различные продукты, а именно СО 2 , карбоновые кислоты и кетоны. Схема окисления алкенов различного строения приведена ниже.





Для иллюстрации пользования этой схемой приведён пример окисления 2-метилпентена перманганатом калия в сернокислой среде. Согласно схеме окисления конечными органическими продуктами для данного алкена являются карбоновая кислота и кетон:

Полуреакции для этого процесса:
 Другой пример: окисление 2-этилбутена-1 дихроматом калия в серной кислоте. В соответствии с правилами схемы окисления в этом случае получаются кетон и углекислый газ:
Другой пример: окисление 2-этилбутена-1 дихроматом калия в серной кислоте. В соответствии с правилами схемы окисления в этом случае получаются кетон и углекислый газ:


Третий пример: окисление цис- 3,4,5-триметилгептена-3 висмутатом натрия в разбавленной азотной кислоте. В соответствии с правилами схемы окисления в данном случае получаются два кетона:


1.5 Озонолиз
Озонолизом называется двухстадийный процесс, на первой стадии которого к алкену присоединяется озон и образуется озонид, а на второй стадии этот озонид либо медленно разрушается водой с образованием перекиси водорода, альдегидов и кетонов, либо быстро восстанавливается цинковой пылью с образованием оксида цинка и тех же альдегидов и кетонов.
Ниже приведён пример озонолиза 3-метил-цис -гептена-3.
При озонолизе можно получить два различных кетона:

В качестве одного из продуктов окисления можно получить формальдегид (метаналь), если в реакцию взять терминальный алкен:

2. Реакции присоединения по двойной связи алкенов.
По двойной связи алкенов могут присоединять как неполярные, так и полярные молекулы.
Неполярные: Н 2 , Cl 2 , Br 2 , J 2 . Фтор F 2 не присоединяется к алкенам, а сжигает их до СF 4 и HF:
СН 3 – СН = СН − СН 3 + 12 F 2 → 4 CF 4 + 8 HF
2.1 Присоединение водорода.
Присоединение происходит только в присутствии катализатора. Чаще всего в промышленности используется палладий или платина, которые легко регенерируются путём прокаливания. Никель практически не используется, так как в условиях обычного прокаливания он превращается в оксид, восстанавливать который экономически не выгодно.
СН 3 – СН = СН 2 + Н 2 СН 3 – СН 2 – СН 3
2.2 Присоединение хлора.
Идёт к двум атомам при двойной связи. Получаются дихлорпроизводные алканов. Реакция может протекать как водном растворе при комнатной или более низких температурах, так и в органических растворителях, например, тетрахлорметане CCl 4 или дихлорэтане C 2 H 4 Cl 2:
2.3 Присоединение брома.
Проходит аналогично как с бромной водой при температурах до 0 0 С, так и в тех же органических растворителях. В последнем случае реакция может проходить и при температуре до – 25 0 С, то есть на морозе.
Реакция с бромом является качественной на присутствие алкенов в газообразных и жидких смесях, так как сопровождается обесцвечиванием оранжевых бромных растворов:
2.4 Реакция с йодом.
Реакция широко используется для определения общей ненасыщенности жиров, которые являются производными ненасыщенных жирных кислот, содержащих двойные связи, как в алкенах:


Массу йода в граммах, пошедшую на полное йодирование 100 г жира, называют йодным числом. Чем оно выше, тем полезнее жир для человека, так как только из полиненасыщенных жирных кислот организм синтезирует гормоны. Примеры йодных чисел: пальмовое масло – 12, бараний жир – 35, оливковое масло – 80, соевое масло – 150, жир сельди – 200, тюлений жир - 280
2.5 Реакции с полярными молекулами.
К полярным молекулам типа Н-А относятся следующие: H-F, H-Cl, H-Br, H-J, H-OH,
H-O-R(спирты) и карбоновые кислоты –
Присоединение хлороводорода и других полярных молекул идёт по, то есть атом водорода из полярной молекулы преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи, а остаток А к другому атому при двойной связи.

Таким образом реакция малоселективная.
При увеличении разности в гидрогенизированности селективность в реакции возрастает. Действительно разница в гидрогенизированности у атомов 1 и 2 в пропене составляет один атом водорода, и к менее гидрогенизированному атому углерода идёт 85% хлора, тогда как в
2-метилпропене разница в гидрогенизированности у атомов 1 и 2 составляет уже два атома водорода и к атому 2 идёт более 98% хлора:
Аналогично идет присоединение HF, HBr, HJ:

Иначе идет присоединение HBr (и только HBr, а не HCl, HF и HI) в присутствии перекиси водорода H 2 O 2:
Эта реакция называется присоединением HBr по Карашу. Селективность в ней практически меняется на обратную в сравнении с таковой для присоединения HBr в отсутствии перекиси водорода (по правилу Марковникова).
Очень интересна реакция алкенов с хлором при 500 О С. В этих условиях реакция присоединения хлора по двойной связи обратима, более того равновесие в ней сильнейшим образом смещено в сторону исходных веществ. Наоборот гораздо более медленная, но необратимая реакция радикального замещения в аллильное положение, то есть рядом с двойной связью идёт до конца:

Эта реакция имеет большое практическое значение. Например, одна из стадий многотоннажного промышленного синтеза глицерина – хлорирование пропена до
3-хлорпропена-1.
При присоединении воды к алкенам в присутствии каталитических количеств серной или ортофосфорной кислот получаются спирты. Присоединение идет по правилу Марковникова:

При присоединении спиртов к алкенам получаются простые эфиры:


Эти изомерные эфиры можно назвать и как производные алканов, содержащие алкокси-заместители, и как простые эфиры. В первом случае выбирается самая длинная цепь из атомов углерода и нумеруется с той стороны, которая ближе к алкокси-заместителю. Например, для эфира I цепь пронумерованная цифрами в скобках. И соответствующее название тоже в скобках. Для изомера II, наоборот цифрами в скобках пронумерована цепь, начинающаяся от атома углерода, связанного с атомом кислорода. Название в этом случае образуется так: сначала называют более простой радикал, связанный с атомом кислорода, затем более сложный и, наконец, добавляют «овый эфир».
При присоединении карбоновых кислот к алкенам получаются сложные эфиры:


Названия сложных эфиров образуются так: сначала называют углеводородный радикал, связанный с кислородом. При этом за атом номер 1 принимают атом углерода, контактирующий с кислородом. От этого атома нумеруют самую длинную из имеющихся цепей. Группы атомов, не вошедшие в главную цепь, считают заместителями и перечисляют по обычным правилам. Затем добавляют «овый эфир такой-то кислоты».
4.3.б. Присоединение галогеноводородов (гидрогалогенирование)
Другой важной реакций электрофильного присоединения к алкенам является давно известное гадрогалогенирование алкенов.
Ниже приведены типичные примеры присоединения HCl, HBr и HI к различным алкенам.


Влияние алкильных заместителей у двойной связи на скорость присоединения описывается следующей последовательностью:
R 2 C=CHR > RCH=CHR > RCH=CH 2
Это согласуется с таким механизмом, в котором в определяющей скорость стадии реакции происходит образование карбокатиона, поскольку стабильность алкильных катионов убывает в ряду третичный > вторичный > первичный. Таким образом, механизм присоединения должен включать промежуточное образование или свободного карбокатиона, что наблюдается редко, или интермедиата с карбокатионным характером. Последний случай наиболее типичен.
Если бы присоединение происходило через "свободный карбокатион", то реакция была бы совершенно нестереоселективной, так, как алкильные катионы имеют плоское строение. Однако, гидрогалогенирование, как правило, протекает стереоселективно, причем в зависимости от типа алкена может наблюдаться селективное анти -присоединение, селективное син - или смешанное син -анти -присоединение.
Для алкенов, у которых двойная связь не сопряжена с ароматическим кольцом, характерно анти -присоединение галогеноводорода. Анти -присоединение хлористого и бромистого водорода, хлористого и бромистого дейтерия наблюдается для циклогексена, циклопентена, 1,2-диметилгексена, 1,2-диметилпентена, цис - и транс -бутена-2, гексена-3 и многих других простых алкенов и циклоалкенов.

В продукте присоединения одинаковые заместители (метильные группы) расположены по разные стороны средней плоскости циклогексанового кольца, следовательно он относится к транс -ряду. Анти -присоединение трудно совместимо с механизмом, в котором предполагается образование дискретного карбокатиона. Для плоского карбокатиона нуклеофильная атака галогенид-иона равновероятна с обеих сторон плоскости, что должно привести к образованию смеси продуктов син - и анти -присоединения. Кинетика гидрогалогенирования алкенов также указывает на более сложный механизм присоединения. Для несопряженных алкенов скорость реакции описывается уравнением третьего порядка со вторым порядком по галогеноводороду, т. е. соответствует Ad E 3-механизму.
v = k [алкен] 2
Анти-присоединение и второй порядок реакции по галогеноводороду хорошо согласуется с Ad E 3-механизмом, в котором алкен взаимодействует с двумя молекулами галогеноводорода, одна из которых выполняет функцию электрофильного, а другая - нуклеофильного агента.

Такой тримолекулярный механизм предполагает, что первоначально образуется комплекс алкена и одной молекулой галогеноводорода с последующей атакой второй молекулы НХ на этот комплекс с анти -стороны без образования дискретного карбокатиона. Следует особо отметить, что любой тримолекулярный механизм должен состоять из двух последовательных стадий, поскольку одновременно столкновение трех молекул крайне маловероятно.

Анти-присоединение свидетельствует о предпочтительной нуклеофильной атаке галогеноводорода со стороны противоположной той, откуда происходит протонирование алкена. Вместо галогеноводорода функцию нуклеофильного агента в конечной стадии может выполнить и галогенид-ион. Действительно, скорость реакции обычно возрастает прямо пропорционально концентрации галогенид-иона, введенного в реакционную смесь в виде галогенидов тетраалкиламмония NR 4+ X - или лития LiX. В этом случае наблюдается стереоспецифическое анти -присоединение.
Для алканов, у которых двойная связь сопряжена с ароматическим кольцом, характерно син -присоединение или смешанное син -анти -присоединение галогеноводорода, например:

Син-присоединение является доминирующим процессом для цис - и транс -изомеров 1-фенилпропена, 1-фенил-4-алкилциклогексенов, аценафтилена, индена. При протонировании таких алкенов образуются карбокатионы бензильного типа, которые стабильнее чисто алкильных катионов, возникающих при протонировании обычных алкенов и циклоалкенов. Кинетика реакции в этом случае обычно описывается более простым уравнением второго порядка v = k[алкен], т. е. соответствует бимолекулярному Ad E 2-механизму. Ad E 2-Механизм предполагает образование ионной пары, включающей карбокатион и галогенид-ион.

Нельзя ожидать, что механизм присоединения с участием ионных пар будет отличаться высокой стереоселективностью. Если ионная пара превращается в конечный продукт быстрее, чем происходит вращение вокруг простой углерод-углеродной связи, конечным результатом будет син -присоединение, где протон и галогенид-ион присоединяется с одной и той же стороны двойной связи. В противном случае наблюдается образование продуктов как син - так и анти -присоединения НХ. Такой случай реализуется при гидрогалогенировании пара -замещенных стиролов Z-C 6 H 4 -CH=CH 2 . Наблюдаемая здесь закономерность заключается в том, что син -присоединение характерно лишь для тех олефинов, которые при протонировании дают относительно стабильный карбокатион, т. е. в случае донорных заместителей Z.
Для реакций гидрогалогенирования, протекающих по Ad E 2-механизму характерна конкуренция процессов сопряженного присоединения и перегруппировок, поскольку в качестве интермедиата образуется карбокатион или ионная пара.

В качестве примера перегруппировок с 1,2-миграцией алкильной группы и гидрид-иона приведем реакции гидрогалогенирования соответственно трет-бутилэтилена и изопропилэтилена.

При проведении этой же реакции без растворителя на холоду (-78 0 С) образуется смесь 33% нормального и 67% аномального (перегруппированного) продуктов присоединения.

4.3.в. Ориентация. Правило Марковникова
В отличие от симметричных электрофилов (Hal 2), галогеноводороды представляют собой несимметричные электрофильные реагенты. Присоединение любого несимметричного электрофила (HBr, ICl, H 2 O, Hg(OAc) 2 и т. д.) к несимметричному алкену в принципе могло бы дать смесь двух альтернативных продуктов, однако на практике обычно образуется только один из них. В качестве примера рассмотрим присоединение бромистого водорода к пропилену.

Еще в 1870 г. В.В. Марковников сформулировал эмпирическое правило, согласно которому несимметричные алкены присоединяют НХ таким путем, что преимущественно образуется продукт, в котором водород присоединяется к наименее замещенному, а Х - к наиболее замещенному концу двойной связи.
Обычно правило Марковникова объясняют различием в стабильности двух альтернативных карбокатионов. Например, в приведенном выше примере нормальный н -пропильный катион значительно менее стабилен, чем изопропильный катион, и поэтому реакция идет по второму пути.
Правило Марковникова первоначально использовалось только для случаев присоединения НХ к углеводородным субстратам, но в принципе его можно распространить и на реакции других замещенных алкенов. Так, присоединение НCl к CF 3 CH=CH 2 дает "анти -марковниковский" продукт CF 3 CH 2 CH 2 Cl. Этого и следовало ожидать, поскольку катион CF 3 CH+ CH 3 менее стабилен, чем катион CF 3 CH 2 CH 2+ из-за сильного (-I)-эффекта CF 3 -группы. Преимущественно образуется катион CF 3 CH 2 CH 2+ , но он тоже, хотя и в меньшей степени дестабилизирован индуктивным эффектом CF 3 -группы, вследствие чего присоединение HCl к трифторметилэтилену идет значительно медленнее, чем присоединение к незамещенному этилену.
По аналогичной причине катионы винилтриалкиламмония присоединяют HBr также против правила Марковникова:
Присоединение НХ к алкенам, имеющим сильные (-I) и (-M)-заместители, например, к акрилонитрилу или нитроэтилену также должно идти против правила Марковникова. Однако в этом случае двойная связь настолько сильно дезактивирована по отношению к электрофильным реагентам, что эти реакции идут лишь в очень жестких условиях. Хлористый винил СН 2 =СНСl всегда дает исключительно "марковниковские аддукты". Например, при его реакции с HCl образуется только 1,1-дихлорэтан (геминальный дихлорид) CH 3 CHCl 2 . Хлор, аналогично CF 3 -группе имеет сильный (-I)-эффект, и на первый взгляд, кажется, что по этой причине присоединение должно иметь антимарковниковскую ориентацию, т. к. катион + CH 2 CH 2 Cl должен быть более стабильным, чем катион СН 3 СН + Cl. Однако, в отличие от CF 3 -группы, хлор кроме (-I)-эффекта обладает также противодействующим ему (+М)-эффектом (т. к. имеет неподеленные пары). Опыт показывает, что величина мезомерного эффекта вполне достаточна, чтобы понизить энергию 1-хлорэтильного катиона ниже уровня энергии 2-хлорэтильного катиона, в котором +М-эффект не проявляется.

II. С позиций теории резонанса строение 1-хлорэтильного катиона может быть представлено следующим образом:
Тем не менее, присоединение к хлористому винилу происходит медленнее, чем к этилену в тех же условиях, т. е. по суммарному эффекту (-I > +M) хлор остается электроноакцепторным заместителем по сравнению с водородом, а 1-хлорэтильный катион менее стабилен, чем С 2 Н 5 + . Аналогичным образом реагируют с НХ и другие винилгалогениды.
Виниловые эфиры CH 2 =CHOR присоединяют НХ (X=Hal) по правилу Марковникова с гораздо большей скоростью, чем все перечисленные выше замещенные алкены. Это связано со значительным +М-эффектом RО-группы. В отличие от атома хлора, RО-группа по суммарному электронному эффекту (+М > -I) является сильным электронодонорным заместителем, эффективно стабилизирующим соседний карбокатионный центр. Строение карбокатиона в этом случае также может быть представлено в виде набора двух резонансных структур
Атака оксониевого катиона галогенид-анионом приводит к образованию -галогенэфиров типа СН 3 СН(Hal)OR.
4.3.г. Гидратация алкенов
Кислотно-катализируемая гидратация алкенов приводит к образованию спиртов. Направление гидратации алкенов определяется правилом Марковникова, поэтому предполагается, что в качестве промежуточной частицы в этой реакции образуется карбокатион.
Склонность вторичных алкильных карбокатионов к перегруппировкам мешает использованию гидратации алкенов для получения вторичных спиртов.

Этот метод в лаборатории нашел ограниченную область применения только для получения третичных спиртов. Реакция гидратации в этом случае в значительной степени обратима и третичные спирты образуются с низкими выходами (40-45%).


Гидратация простейших алкенов - этилена и пропилена - представляет собой важный промышленный метод получения этилового и изопропилового спиртов.
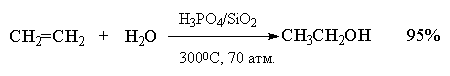
В лабораторной практике прямая гидратация алкенов не нашла широкого применения как вследствие жестких условий, так и благодаря образованию значительного количества изомерных спиртов. В настоящее время для региоселективного получения спиртов из алкенов обычно используется родственная реакция гидроксимеркурирования - демеркурирования.
4.3.д. Гидроксимеркурирование-демеркурирование
Электрофильная атака на двойную связь алкена может осуществляться ионами металлов, среди которых особое положение занимает катион ртути (II). Ацетат ртути в очень мягких условиях при 20 0 С присоединяется к алкенам в водном тетрагидрофуране (ТГФ) или в водной уксусной кислоте с образованием ртутьорганических соединений. Присоединение ацетата ртути по двойной связи протекает региоспецифично в строгом соответствии с правилом Марковникова, т. е. катион ртути присоединяется к наименее замещенному атому углерода.
Связь С-Hg в ртутьорганических соединениях может быть легко расщеплена под действием боргидрида натрия NaBH 4 , с образованием ртути и новой связи С-Н. Предполагается, что в качестве нестабильного интермедиата при этом получается алкилмеркургидрид, который далее разлагается с выделением металлической ртути по радикальному механизму.

Суммарно этот двухстадийный процесс гидроксимеркурирования-демеркурирования в конечном итоге представляет собой региоспецифичную гидратацию алкена по правилу Марковникова в исключительно мягких условиях, когда образование побочных продуктов сведено к предельно возможному минимуму. Это можно наглядно проиллюстрировать с помощью следующих примеров, в которых суммарный выход продуктов реакции составляет 90-98%. Приведенные цифровые данные в этом случае обозначают не выходы образующихся соединений, а их соотношение в смеси.

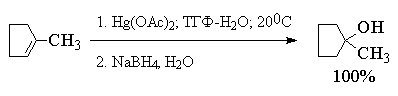


Как видно из приведенных выше примеров гидроксимеркурирование-демеркурирование алкенов в большинстве случаев обеспечивает региоспецифическую гидратацию алкенов с образованием практически только одного из двух изомерных спиртов. Следует отметить, что нет никакой необходимости в выделении ртутьорганического соединения, и оба процесса могут быть проведены непосредственно один за другим.
Гидроксимеркурирование несимметричных алкенов, по-видимому, начинается с атаки катиона AcOHg + и образования в качестве интермедиата несимметричного циклического меркуриниевого катиона (аналога несимметричного галогенониевого иона), который затем раскрывается в результате нуклеофильной атаки водой по наиболее замещенному атому углерода, несущему больший положительный заряд.
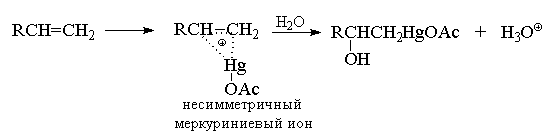
Мостиковый меркуриниевый ион можно зафиксировать в ненуклеофильной сильнокислой среде даже при 20 0 С при присоединении более сильного электрофильного агента - трифторацетата ртути в смеси фторсульфоновой кислоты и пятифтористой сурьмы.

Меркуриниевый катион может расщепляться не только при действии воды, но и других электронодонорных растворителей: спиртов, уксусной кислоты, ацетонитрила и др. Конечным продуктом реакции в этом случае будут соответственно простые эфиры, ацетаты или N-замещенные амиды уксусной кислоты, например:

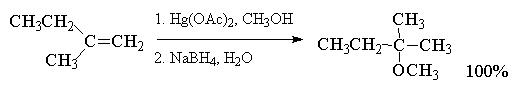
При использовании в реакции алкоксимеркурирования-демеркурирования разветвленных вторичных или третичных спиртов более эффективными, чем ацетат ртути, являются трифторацетат Hg(OCOCF 3) 2 или трифлат ртути Hg(OSO 2 CF 3) 2 .

Таким образом, гидрокси- и алкоксимеркурирование-демеркурирование - это один из лучших препаративных методов синтеза спиртов и простых эфиров с разветвленными алкильными радикалами.
Присоединение солей ртути к алкенам представляет собой наиболее яркий пример реакции сопряженного присоединения к двойной связи, где роль внешнего нуклеофильного агента выполняет растворитель. Стереохимия двойного процесса гидроксимеркурирования-демеркурирования зависит от стереохимического результата каждой отдельной стадии. Для гидроксимеркурирования характерно анти -присоединение, как и для других реакций с участием циклического катиона. Однако радикальное демеркурирование не отличается высокой стереоселективностью. Поэтому весь процесс в целом также нестереоспецифичен.
4.3.е. Присоединение алкенов (катионная димеризация и полимеризация алкенов)
Наиболее интересным примером такого типа реакций является димеризация и полимеризация изобутилена в присутствии серной кислоты.

Техническое название этой смеси алкенов - "диизобутилен". Данная реакция протекает по катионному механизму, сходному с механизмом присоединения минеральных кислот к двойной связи алкенов. На первой стадии протон присоединяется к молекуле изобутилена с образованием относительно стабильного трет -бутилкатиона. Далее образовавшийся трет -бутилкатион (кислота Льюиса) реагирует с молекулой изобутилена (основание Льюиса) с образованием нового стабильного третичного октильного катиона.

В данных условиях под действием оснований (H 2 O, HSO 4 - -ионы) октильный карбокатион быстро теряет протон и превращается в смесь изомерных пентенов, т. к. отрыв протона происходит из двух различных положений:

Преимущественное образование термодинамически менее стабильного алкена - 2,4,4-триметилпентена-1 (80% в реакционной смеси) связано с большей пространственной доступностью для атаки основанием атомов водорода метильных групп, по сравнению с атомами водорода метиленовой группы. В промышленности "диизобутилен" гидрируют на Ni-Ренея и получают "изооктан" (техническое название углеводорода 2,2,4-триметилпентана), используемый в качестве высокооктанового топлива для двигателей внутреннего сгорания.
При высоких концентрациях серной кислоты (более 80%) происходит катионная полимеризация изобутилена с образованием полимера, называемого полиизобутиленом (-CH 2 C(CH 3) 2 -) n . Этот каучукоподобный полимер используют для получения антикоррозионных и гидроизоляционных покрытий, герметиков и др.
Кроме изобутилена, по катионному механизму полимеризуются 3-метилбутен-1, виниловые эфиры и некоторые производные стирола, способные образовывать сравнительно устойчивые карбокатионы. В качестве катализаторов катионной полимеризации также используют фтористый водород и кислоты Льюиса: BF 3 , AlCl 3 , AlBr 3 и др. в присутствии очень малых количеств воды.
4.3.ж. Присоединение алканов (алкилирование алкенов)
Другой промышленный метод синтеза "изооктана" основан на взаимодействии изобутилена с избытком изобутана в присутствии концентрированной серной кислоты или в безводном фтористом водороде при 0 10 0 С.

Эта реакция также протекает по катионному механизму и, что особенно интересно, является примером цепного катионного процесса. Сначала изобутилен в условиях реакции димеризуется с образованием третичного октильного катиона (CH 3) 3 CCH 2 C + (CH 3) 2 . Подробно механизм его образования изложен в предыдущем разделе. Далее происходит быстрый перенос водорода (в виде гидрид-иона) от изобутана к октильному катиону с образованием молекулы "изооктана" и нового трет-бутилкатиона, который в свою очередь быстро реагирует с изобутиленом с образованием нового октильного катиона и т. д.

Кроме синтеза "изооктана", такой метод алкилирования используется в нефтехимической промышленности для синтеза высококипящих разветвленных углеводородов из разветвленных алкенов и алканов низкокипящих фракцией термического крекинга.